ニュース
NEWS
抗がん剤耐性を獲得したがん細胞に対する治療法開発へ期待
―がん抑制因子p53の機能低下がもたらす 抗がん剤応答への異常を新たに発見―
概要
甲南大学(学長:中井伊都子/兵庫県神戸市)フロンティアサイエンス学部の川内 敬子准教授、取井 猛流大学院生、杉本 渉大学院生(研究当時)、伊藤 功彦大学院生(研究当時)と、金沢工業大学(学長:大澤敏/石川県野々市市)応用バイオ学科の平田 宏聡教授の研究グループは、日本医科大学先端医学研究所の研究グループとの共同研究で、がん抑制因子p53の機能低下時に抗がん剤に対する異常な細胞応答が引き起こされることを新たに発見しました。アクチンは細胞に多量に存在するタンパク質ですが、この応答では、抗がん剤によりDNAの損傷を受けた細胞の核内でアクチンの線維化が起こります。さらに研究グループは、p53の機能低下による核内でのアクチンの線維化を利用して、がん細胞での遺伝子の転写を抑制させ、抗がん剤の細胞毒性を高める方法を発見しました。本研究の成果は、核内のアクチンをターゲットとした新たながん医療への応用が期待されます。
この成果は国際科学誌、Springer Nature 『Cell Death & Disease』(Published:25 November 2023)で発表されました。
研究のポイント
・p53の機能が低下した細胞では、抗がん剤処理により核内でアクチン線維が形成されることを発見しました。
・p53は、抗がん剤処理に応答してタンパク質分解酵素カスパーゼの活性化を促すことで核内のアクチンの線維化を抑えることが分かりました。
・線維化したアクチンに結合するLifeactペプチドは、p53の機能低下した細胞において、抗がん剤処理で形成される核内のアクチン線維の構造を変えることを発見しました。
・Lifeactペプチドは、DNAの塩基配列をコピーして合成されるRNAの転写量を減少させることを発見しました。
・p53の機能低下は正常細胞では通常みられないことから、p53機能低下時のみに形成される核内アクチン線維に介入することによる転写の阻害とそれによる細胞増殖の抑制は、がん細胞に対してより特異的に抗がん剤の効果を強められる副作用を抑えた治療法の開発につながることが期待できます。
研究の背景
p53は、DNA損傷に対する細胞応答において中心的な役割をになうことがよく知られています。抗がん剤によりDNAが損傷を受けると、p53は活性化され、増殖の停止やDNAの修復、細胞死(アポトーシス)の誘導などといった機能を発揮します。一方、がんにおいては高頻度にp53遺伝子の変異がみられます。遺伝子の変異によりp53の機能が喪失したがん細胞では、これら細胞の反応が抑えられるため、化学療法などの治療に対して感受性が低くなります。したがって、p53の機能が低下した細胞に抗がん剤の効果を増強する方法の開発は、抗がん剤耐性を克服できる治療法につながると考えられます。最近の研究で、DNAが損傷を受けると、核内にてアクチン線維が形成されることが分かってきました。核内のアクチンは、転写の調節や損傷したDNA領域の修復において機能を果たすことが明らかにされつつあります。そこで研究グループは、p53の機能低下が核内のアクチン線維の形成に及ぼす影響を調べることで、抗がん剤耐性のメカニズムの解明や新たな治療標的の発見につながる可能性があると考え、解析を行いました。
具体的な研究成果の内容
はじめに、p53の機能を低下させるため、p53に対するshRNAを用いてp53の発現を恒常的に低下させた乳がん由来の細胞株MCF-7細胞(p53ノックダウン細胞)を作成しました。核内のアクチン線維の選択的な可視化には、アクチン結合性ペプチドLifeactに核移行シグナルペプチド(NLS)と蛍光タンパク質GFPを付加したプローブ(nLifeact-GFP)を用いました。p53ノックダウン細胞にnLifeact-GFPを発現させ、抗がん剤で処理すると、核内に太く長い束状のアクチン線維が形成されました(Fig.1a)。一方、p53に対するshRNAを発現させていないMCF-7細胞(コントロール細胞)では、このようなアクチン線維構造は見られませんでした。核内のアクチン線維を検出する他のプローブであるnAC-GFP(Fig.1b)やYFP-nβ-actin(Fig.1c)を使用した場合でも、p53ノックダウン細胞においてのみ、抗がん剤処理により核内にアクチン線維が形成されることが確認されました。p53は、タンパク質分解酵素であるカスパーゼを活性化することが知られています。広汎カスパーゼ阻害剤Q-VD-OPhまたはカスパーゼ1阻害剤Z-YVAD-FMKを抗がん剤とともに処理すると、p53を発現したコントール細胞においても核内にアクチン線維が形成されるようになりました(Fig.1d)。すなわち、p53の機能低下は、カスパーゼの活性を抑えることで核内アクチン線維の形成の促進することが示唆されました。
さらに研究グループは、核内アクチンの可視化プローブ3種類で観察されるアクチン線維構造が異なることに気がつきました。とくにnLifeact-GFPを用いた場合、アクチン線維は太い束状となり、それに沿ってクロマチン構造が線状に配置することを見つけました(Fig.2a)。クロマチンの構造は、遺伝子の発現制御において非常に重要な役割を果たしています。このため、nLifeact-GFPを発現したp53機能低下細胞では転写の異常が起きていることが予想されました。実際にこの細胞では、転写活性化マーカーであるアセチル化したヒストンH3の量が減少していること(Fig.2b)、またRNAの合成が低下していること(Fig.2c)が確認されました。これらのことから、nLifeactペプチドは、p53の機能が低下したがん細胞に対して核内アクチン線維の構造を変化させ、転写反応を抑制する効果を有すると考えられます。
今後の研究展開および波及効果
本研究では、p53の機能が低下すると、抗がん剤による核内アクチン線維の形成が促進されることを発見しました(Fig.3)。先行研究において、核内アクチン線維は転写反応を促進することが報告されています。遺伝子の転写は細胞が増殖するために必須のプロセスであることから、p53の機能低下にともなう核内アクチン線維の形成は、抗がん剤耐性に関連する遺伝子を発現させることで抗がん剤存在下でのがん細胞の増殖に関与している可能性があります。一方で、Lifeactを核内に発現させると、p53の機能が低下したがん細胞で、異常な構造をもつ核内アクチン線維が形成され、転写反応が抑えられることを見出しました。この結果は、p53が機能低下し抗がん剤耐性となったがん細胞の増殖をLifeactにより抑制できる可能性があることを示しています。今後、当研究チームは、Lifeactペプチドの細胞核内への取り込み量を高める方法を研究し、抗がん剤耐性を克服するがん治療の新たな道筋を切り開いていきます。
用語説明
p53:がんの発生や進行を抑える最も代表的なタンパク質。さまざまな遺伝子の転写を調節し、細胞の生存、増殖、老化、アポトーシスなどのプロセスに重要な役割を果たす。p53タンパク質をコードするp53遺伝子は、半数のがんで変異している。
アクチン:細胞内に多量に存在するタンパク質。単量体のアクチンと、それらが重合した線維状のアクチンの2状態が存在する。古くから細胞運動において中心的な役割を果たすことが知られていたが、最近の研究で染色体の構造や転写の制御に関与していることも分かってきている。
Lifeact:アクチン線維に特異的に結合する17アミノ酸からなるペプチド。
nAC-GFP:アルパカ由来のアクチン特異的VHH抗体(Actin chromobody:AC)にNLSとGFPを付加した核内のアクチンを可視化するためのプローブ
YFP-nβ-actin:ほとんどすべての細胞に発現しているアクチンのアイソフォームであるβ-actinにNLSと蛍光タンパク質YFPを付加した核内のアクチンを可視化するためのプローブ
カスパーゼ:アポトーシス(プログラム細胞死)において中心的な役割を果たすタンパク質分解酵素。ヒトにおいて14種類のカスパーゼが同定されている。
DNA:デオキシリボ核酸の略。DNAは、染色体の主要な構成要素であり、遺伝情報を保持する。
RNA:リボ核酸の略。RNAは、DNAの塩基配列をコピーして合成され、その情報がタンパク質合成などに利用される。
shRNA:ショートヘアピンRNAの略。RNA干渉によって標的遺伝子の発現を抑制するのに用いられる。
クロマチン:DNAとタンパク質ヒストンの複合体。クロマチンの構造は、遺伝子の発現に密接に関係している。
転写:DNAの情報がRNAへとコピーされる過程のこと。
核移行シグナル (NLS) ペプチド:
タンパク質を核へ輸送するためのシグナルとして働くアミノ酸配列。
GFP:緑色蛍光タンパク質。
アセチル化ヒストンH3:
クロマチンの構成要素であるタンパク質ヒストンH3がアセチル化したもの。本研究では転写活性化マーカーとして知られるリジン9番目がアセチル化したヒストンH3を示す。
エチニルウリジン(EU):
核酸構造の特殊な修飾ヌクレオシド。EUは新規合成されるRNAに取り込まれるため、細胞内のRNA合成量を追跡することができる。
図について
[Fig.1]p53の発現抑制は抗がん剤による核アクチン線維形成を促進する
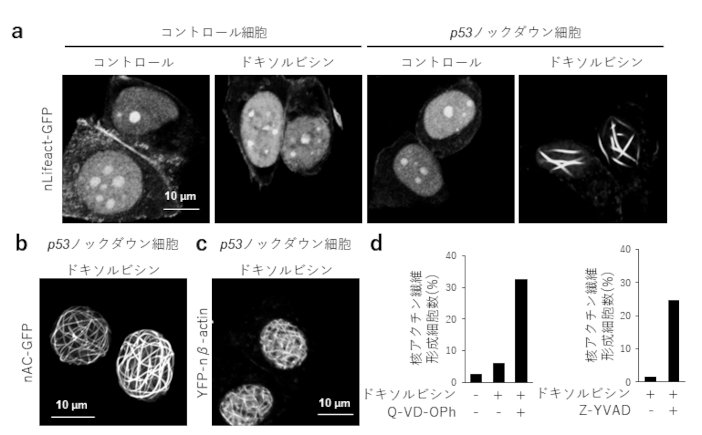
(a) nLifeact-GFP、(b)nAC-GFP、 (c)YFP-nβ-actinを細胞に発現させました。p53ノックダウン細胞でのみ、抗がん剤ドキソルビシン処理により、核内にアクチン線維が形成されることを確認しました。
(d) カスパーゼの阻害剤Q-VD-OphまたはZ-YVADをドキソルビシンと共に処理するとコントロール細胞において核アクチン線維の形成を確認しました。
[Fig.2]nLifeactによる核アクチン線維の束化によるDNA構造の変化と転写抑制効果
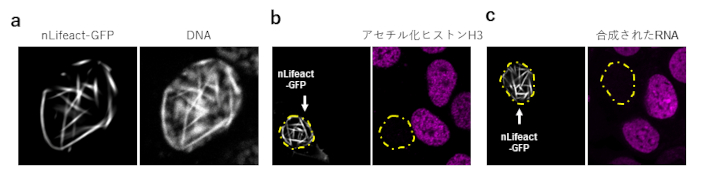
nLifeact-GFPを発現させたp53ノックダウン細胞では核アクチン線維が太い束状となり、それに沿ってクロマチン構造が線状に配置しました (a)。またこの細胞ではヒストンH3のアセチル化レベルが減少し (b)、RNAの合成量が低下しました (c)。
[Fig.3]抗がん剤が誘導する核アクチン線維の形成におけるp53の役割と核アクチン線維結合Lifeactペプチドによる遺伝子発現制御モデル
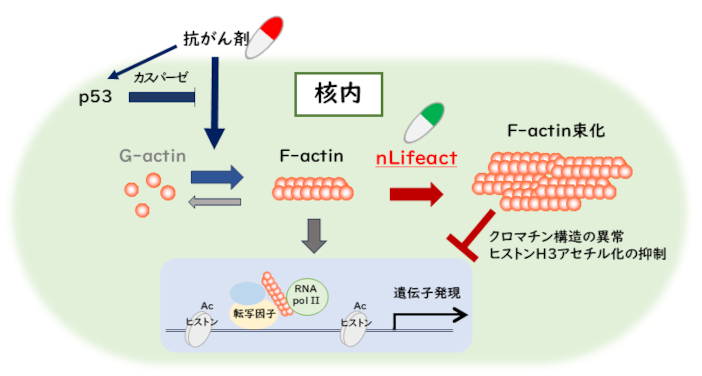
発表雑誌
[学術誌名]Springer Nature 『Cell Death & Disease』
https://doi.org/10.1038/s41419-023-06310-0
[論文タイトル]Loss of p53 function promotes DNA damage-induced formation of nuclear actin filaments
[著者]Takeru Torii*1, Wataru Sugimoto*1, Katsuhiko Itoh*1, Natsuki Kinoshita1, Masaya Gessho1, Toshiyuki Goto1, Ikuno Uehara2, Wataru Nakajima2, Yemima Budirahardja1, Daisuke Miyoshi1, Takahito Nishikata1, Nobuyuki Tanaka2, Hiroaki Hirata3†, Keiko Kawauchi1,2†
1 甲南大学フロンティアサイエンス学部、2 日本医科大学先端医学研究所、3 金沢工業大学応用バイオ学科 *共同第一著者、†共同責任著者
主な競争的研究資金
本研究は、日本学術振興会科研費(JP18K06231, JP19J21096, JP20K12596, JP21H05127, JP21K06158)、国立研究開発法人科学技術振興機構 次世代研究者挑戦的研究プログラム(JPMJSP2117)、甲南学園平生太郎基金科学研究奨励助成金を中心とした支援のもとで行われました。
【関連ページ】
